1 實(shí)驗(yàn)?zāi)康暮鸵?nbsp; 掌握碘(Iodine)量法測定(gage)溶解氧(dissolved oxygen)(Oxygen)的方法原理,。
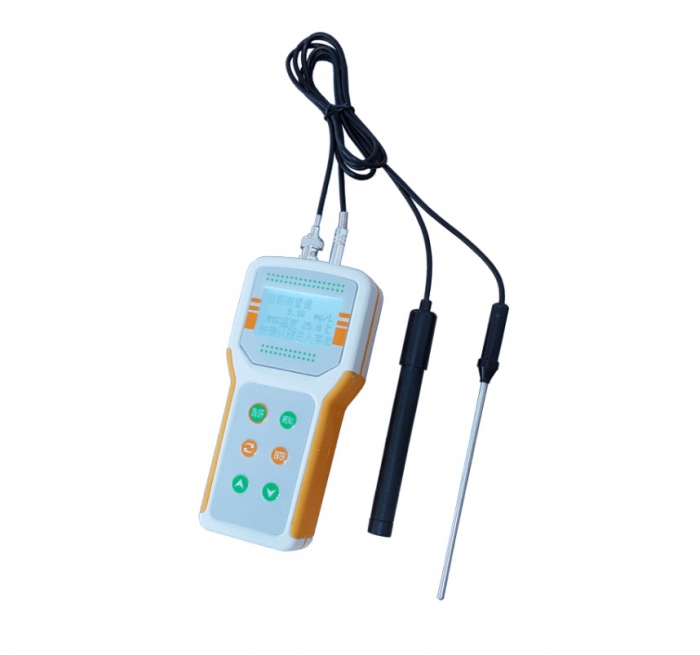
溶解氧測定儀是測定水中溶解氧的裝置,,工作原理是氧透過隔膜被工作
電極還原,,產(chǎn)生與氧濃度成正比的擴(kuò)散電流,通過測量此電流,,得到水中溶解氧的濃度,。 2 方法原理 溶解于水中的分子態(tài)氧稱為溶解氧。水中溶解氧的含量與大氣壓力,、水溫及含鹽量等因素(factor)有關(guān),。大氣壓力下降、水溫升高,、含鹽量增加,,都會(huì)導(dǎo)致溶解氧含量降低(reduce)。 清潔地表水溶解氧接近飽和,。當(dāng)有大量藻類繁殖時(shí),,溶解氧可能過飽和;當(dāng)水體受到有機(jī)物質(zhì),、無機(jī)物質(zhì)污染(pollute)時(shí),,會(huì)使溶解氧降低,甚**趨于零,,此時(shí)厭氧細(xì)菌(fungus)繁殖活躍,,水質(zhì)惡化。水中溶解氧低于3-4mg/L時(shí),,許多魚類呼吸困難,;繼續(xù)減少,則會(huì)窒息死亡,。在這種情況下,,厭氧菌繁殖并活躍起來,有機(jī)物發(fā)生腐敗作用,,會(huì)使水源有臭味,。一般規(guī)定水體中的溶解氧**少在4mg/L以上。在廢水生化處理過程中,,溶解氧也是一項(xiàng)重要控制指標(biāo),。 測定水中溶解氧的方法有碘量法及其修正法和氧
電極法。清潔水可用碘量法,;受污染和地面水和工業(yè)廢水必須用修正的碘量法或氧
電極法,。 水樣中加入硫酸錳(manganese)和堿性碘化鉀(Potassium),,在溶解氧的作用下,,生或氫氧化(oxidation)錳沉淀,此時(shí)氫氧化錳性質(zhì)極不穩(wěn)定,,繼續(xù)氧化生成錳酸,。 MnCl2+2NaOH=Mn(OH)2↓+2NaCl 2Mn(OH)2↓+O2=2MnO(OH)2↓ MnO(OH)2+Mn(OH)2=2H2O+MnMnO3↓ 棕黃色沉淀,,溶解氧越多,沉淀顏色越深,。加酸后使已經(jīng)化合的溶解氧(以MnMnO3的形式存在)與溶液中所存在的碘化鉀起氧化作用而釋出碘,。 2KI+H2SO4(濃)=2HI+K2SO4 MnMnO3+2H2SO4(濃)+2HI=2MnSO4+I2+3H2O 以淀粉(starch)作指示劑,用硫代硫酸鈉標(biāo)準(zhǔn)溶液滴定,,可以計(jì)算(calculate )出水樣中溶解氧含量,。滴定反應(yīng)如下: 2Na2S2O3+I2=Na2S4O6+2NaI
(簡潔原理:水樣中溶解氧(dissolved oxygen)與氯化錳和氫氧化鈉(化學(xué)式:NaOH) 反應(yīng)(reaction),,生成高價(jià)錳棕色沉淀,。
ph計(jì)是指用來測定溶液酸堿度值的儀器,是一種常見的分析儀器,,廣泛應(yīng)用在農(nóng)業(yè),、環(huán)保和工業(yè)等*域。土壤pH值是土壤重要的基本性質(zhì)之一,。
溶解氧測定儀是測定水中溶解氧的裝置,,工作原理是氧透過隔膜被工作電極還原,產(chǎn)生與氧濃度成正比的擴(kuò)散電流,,通過測量此電流,,得到水中溶解氧的濃度。加酸(Acerbity)溶解后,,在碘離子存在下即釋出與溶解氧含量相當(dāng)?shù)挠坞x碘,,然后用硫代硫酸鈉標(biāo)準(zhǔn)溶液滴定游離碘,換算溶解氧含量,。) 6 3 試劑(reagent)及其配制 除另有說明,,所用試劑均為分析純,水為蒸餾(still)水(distilled water)或等效純水,。 3.1 氯化錳溶液:稱取210g氯化錳(MnCl2·4H2O),,溶于水,并稀釋**500mL,。 3.2 堿性碘化鉀溶液:稱取250g氫氧化鈉(NaOH),,在攪拌下溶于250mL水中,冷卻后,,加75g碘化鉀(KI),,稀釋**500mL,盛于具橡皮塞的棕色試劑瓶中,。 3.3 硫酸溶液(acid solution)(1+1):在攪拌下,,將50mL濃硫酸(H2SO4,ρ=1.84g/mL)小心地加到同體積的水中,混勻,。盛于試劑瓶中,。 3.4 硫代硫酸鈉溶液[c(Na2S2O3·5H2O)=0.01mol/L]:稱取25g硫代硫酸鈉(Na2S2O3·5H2O),用剛剛煮沸冷卻的水溶解,,加入約2g碳酸鈉,,移入棕色試劑瓶中,稀釋**10L,,混勻,。置于陰涼處。 硫代硫酸鈉溶液的標(biāo)定: 移取10.00mL碘酸鉀標(biāo)準(zhǔn)溶液(c(1/6KIO3)=0.0100mol/L),,沿壁流入碘量瓶中,,用少量水沖洗瓶壁,加入0.5g碘化鉀,,沿壁注入1.0mL硫酸溶液(1+3),,塞好瓶塞,輕蕩混勻,,加少許水封口,,在暗處放置2min。輕輕旋開瓶塞,,沿壁加入50mL水,,在不斷振搖下,用硫代硫酸鈉溶液滴定**溶液呈淡黃色,,加入1mL淀粉溶液,,繼續(xù)滴定**溶液藍(lán)色剛褪去為止。重復(fù)(repeat)標(biāo)定,,**兩次滴定讀數(shù)差小于0.05mL為止,。按式
(1)計(jì)算(calculate )其濃度:
7 ——橡皮管:直徑5~6mm,長20~30cm,; ——滴定管:25或50mL,,分刻度0.05mL; ——錐形燒瓶(flask):容量(Capacity)250mL,; ——碘量瓶:容量250mL,; ——量筒:200mL; ——棕色試劑瓶:500mL,,1000mL,; ——定量加液器:1mL,2個(gè),; ——移液吸管:1mL,; ——一般實(shí)驗(yàn)室常備儀器和設(shè)備(shèbèi),。 5 分析步驟 實(shí)際實(shí)驗(yàn)步驟分成戶外采樣固定和室內(nèi)分析兩部分。 5.1 水樣的現(xiàn)場采集和固定 shou先檢查溶解(solubility)氧采樣瓶是否漏水,。然后,打開水樣瓶塞,,將連接有機(jī)玻璃(是一種通俗的名稱,、縮寫為PMMA)采水器底部的橡皮管另一端插入水樣瓶底部,慢慢注入待測海水(速度過快會(huì)產(chǎn)生氣泡),,直**溢出,,待海水溢出水樣瓶三倍體積(volume)后,抽出橡皮管,,立即用定量加液器(管尖插入液面)依次序注入1.0mL氯化錳溶液和1.0mL堿性碘化鉀溶液,,塞緊瓶塞(瓶內(nèi)不準(zhǔn)有氣泡),按住瓶蓋將瓶蓋上下顛倒不少于20次,。避光保存,,返回實(shí)驗(yàn)室后盡快完成其他測定(gage)步驟。 5.2 實(shí)驗(yàn)室測定步驟
